


Solide
Liquide
Liquide
Vapeur
Où trouve-t-on de l’eau sur notre planète et comment est-elle ?
Étude de la vidéo « AQUA ça sert ? » https://www.youtube.com/watch?v=d5tCOQ6ijlY
Schématise les quatre béchers présents sur le bureau et leur contenu.
|
|
|
|
Solide |
Liquide |
Liquide |
Vapeur |
Le glaçon prend-il la forme du récipient ? Non
L’eau liquide prend-elle la forme du récipient ? Oui
Comment est la surface libre (Surface en contact avec l’air) de l’eau ?
La surface est horizontale
Le gaz occupe-t-il tout l'espace du récipient ? Oui
Exercice 5 p 19 et 13 p 21
Activité le cycle de l'eau.
Question 1. |
Question 2. |
(1) Océan |
Liquide |
(2) Vapeur d'eau |
Gaz |
(3) Nuages |
Liquide |
(4) Pluie |
Liquide |
(5) Neige |
Solide |
(6) Rivière |
Liquide |
(7) Nappe phréatique |
Liquide |
3. s'évapore ; condense ; fond
4. On parle de cycle de l'eau, car on voit le parcours de l'eau et de ses changements d'état qui se répètent sans fin.
Chauffage |
||||
|
Fusion |
|
Vaporisation |
|
État Solide |
|
État liquide |
|
État gazeux |
|
Solidification |
|
Liquéfaction |
|
|
||||
Fin du cahier : Exercice 3 p 19, 4 p 19 et 14 p 31
Activité : Le cycle de l'eau
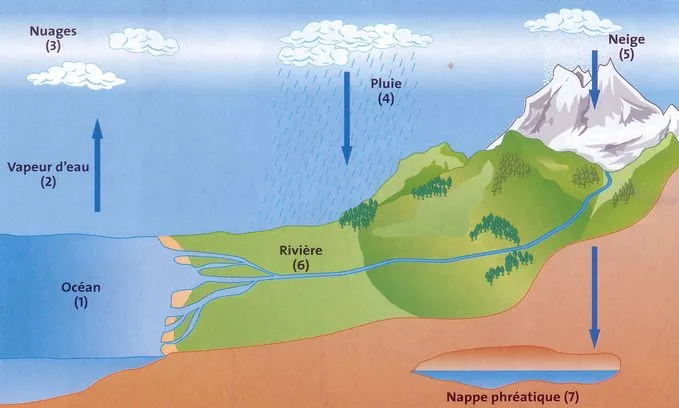
Sous l'action de la chaleur, l'eau des océans (1), des lacs, des rivières s'évapore lentement alors un gaz invisible : la vapeur d'eau (2).
Cette vapeur s'élève dans l'air et rencontre des zones plus froides. Elle se condense et devient de fines gouttelettes d'eau ou de minuscules cristaux de glace qui forment les nuages (3).
L'eau retombe alors sur la Terre sous forme de gouttelettes de pluie (4) ou de flocons de neige (5).
Lorsque les beaux jours reviennent, la neige redevient liquide : elle fond.
Toute l'eau liquide qui arrive sur le sol peut ruisseler, alimenter les fleuves et les rivières (6) ou s'infiltrer dans le sol (7).
Un jour enfin, après un temps plus ou moins long, l'eau retrouvera la mer.
VOCABULAIRE État
de l'eau :
Changement
d'état : Cycle :
|
QUESTIONS
|
Si le pH est < 7 |
La solution est acide |
Si le pH est = 7 |
La solution est neutre |
Si le pH est > 7 |
La solution est basique |
Mesures :
Eau |
pH=7 neutre |
Coca |
pH=3 acide |
Eau savonneuse |
pH=10 basique |
Que se passe-t-il, si on met de l’eau sur du sulfate de cuivre anhydre ?

Observation : La poudre blanche devient bleue au contact de l'eau.
Fin du cahier : Exercice 7 p 50 et 10 p 50
On dispose de quatre liquides : Cola, lait, alcool et huile et de trois solides : pomme, pomme de terre et sucre.
On veut savoir s’ils contiennent de l'eau et si oui quel est leur pH.
|
|
Substances |
Test
au sulfate |
Mesure du pH |
Cola |
Positif |
pH= 3 |
Lait |
Positif |
pH= 6 |
Alcool à brûler |
Positif |
pH = 7 |
Huile |
Négatif |
|
Pomme de terre |
Positif |
pH = 7 |
Pomme |
Positif |
pH = 5 |
Sucre |
Négatif |
|
La masse m est une grandeur, son unité internationale est le kilogramme (kg). En chimie, on utilise souvent le gramme (g).
1 kg = 1000 g
La Tare d'une balance permet de soustraire la masse du bécher au début de la mesure.
On allume la balance
On pose le bécher vide sur la balance
On appuie sur le bouton Tare.
On met l'eau dans le bécher.
On
peut lire directement la masse de l'eau.
m=_62_g = 0,062_kg
Le volume V est une grandeur, son unité internationale est le mètre cube (m3)
En chimie, on utilise souvent le litre (L) et le millilitre (mL)
1 m3 = 1000 L et 1 L = 1000 mL
Mesure
le volume d’eau contenu dans le bécher
V=__mL = __L |
|
La masse volumique ρ est une grandeur, son unité internationale est le kg/m³.
En chimie, on utilise souvent le kg/L ou g/mL.
Reporte dans le tableau suivant tes résultats et déduis-en la masse de 1L d’eau.
|
Eau ( bécher ) |
1L d'eau |
Masse d'eau (kg) |
0,066 |
≈1 |
Volume d'eau (L) |
0,065 |
1 |
Conclusion :
|
ρ rhô |
Exercice 3 p 99, 4 p 99 et 2 p 99
Exercice 5 p 19
a : vapeur d’eau : non visible
b. liquide : forme du récipient et surface horizontale
c. solide : forme du récipient et pas surface horizontale
Exercice 13 p 31
Un gaz occupe tout l’espace disponible
Exercice 3 p 19
Solide : verglas, neige, glace, grêle.
Liquide : pluie, rosée, brume.
Gazeux : vapeur d’eau
Exercice 4 p 19
a. brume : c’est un mélange d’eau liquide et d’air et pas d’eau solide.
b. vapeur d’eau : c’est gazeux et non pas liquide.
Exercice 14 p 31
Il faut une fusion puis une solidification
Exercice 7 p 50
a. Le matériel doit être bien sec pour que l’humidité ne réagisse pas avec le sulfate de cuivre anhydre.
b. La poudre devient bleue. Le test est positif, la banane contient de l’eau.
Exercice 10 p 50
a. Le sirop de citron, le jus d’orange et le lait contiennent de l’eau car la sulfate de cuivre anhydre devient bleue à leur contact.
b. L’huile ne contient pas d’eau.
Exercice 3 p 99
ordre pour peser : c-b-d-a
Exercice 4p99
a : 90 mL b : 94 mL c : 22 cL
Exercice 2p99
m = 9,0 g V= 26-20=6mL ρ=m/V=9/6=1,5g/mL